วันศุกร์ที่ 20 กันยายน พ.ศ. 2562
วันอังคารที่ 17 กันยายน พ.ศ. 2562
ข้อสอบ O-NET ปี 2550
ข้อที่ 1. ข้อใดไม่ใช่หน้าที่ของโปรตีน
1 :
รักษาสมดุลของน้ำและกรด-เบส
2 :
เป็นส่วนประกอบของเอนไซม์ทุกชนิด
3 :
สร้างอิมมูโนโกลบูลิน
4 : ช่วยละลายวิตามิน A D E K
ข้อที่2. สารชนิด
A เมื่อหยดสารละลายเบเนดิกต์ลงไป
แล้วเกิดตะกอนสีแดงอิฐ สารชนิด B เมื่อหยดสารละลายทิงเจอร์ไอโอดีนลงไป
แล้วเกิดสีน้ำเงิน ข้อใดผิด
1 : A คือ มอโนแซ็กคาไรด์
2: B สามารถย่อยสลายด้วยเอมไซม์อะไมเลสแล้วจะได้น้ำตาลแลกโตส
3 :
เมื่อนำ A ไปหมักด้วยยีสต์ จะได้เอทิลแอลกอฮอล์
4 : B เมื่อถูกความร้อนจะสลายเป็นเด็กซ์ตริน
มีสมบัติเหนียวแบบกาว
ข้อที่ 3. ข้อใดไม่ใช่องค์ประกอบของกรดดีออกซีไรโบนิวคลีอิก
( DNA)
1 :
น้ำตาลไรโบส
2 :
อะดีนีน
3 :
หมู่ฟอสเฟต
4 : กรดไรโบนิวคลิอิก (RNA)
ข้อที่ 4. โครงสร้างของDNA สายหนึ่งมีคู่เบสเป็น A C A G ดังนั้นคู่เบสของ DNA อีกสายคือข้อใด
1 : A C A G
2 : C A G A
3 : T G T C
4 : G T T C
ข้อที่ 5. ข้อใดเป็นพอลิเมอร์ทั้งหมด
1 : แป้ง เซลลูโลส น้ำตาล
2 : โปรตีน พอลิเอทิลีน ยางพารา
3 : ไขมัน เตตระฟลูออโรเอทิลีน
ไวนิลคอลไรด์
4 : ไกลโคเจน ซิลิโคน กลูโคส
ข้อที่ 6. พลาสติกชนิดใดไม่ใช่เทอร์โมพลาสติก
1 :
A เป็นพลาสติกที่เมื่อได้รับความร้อนจะอ่อนตัว
2 :
B เป็นพลาสติกที่สามารถนำกลับมาใช้ใหม่ได้
3 :
C เป็นพลาสติกที่สมบัติไม่เปลี่ยนแปลง
4 : D เป็นพลาสติกที่มีโครงสร้างแบบตาข่ายหรือร่างแห
ข้อที่ 7. พิจารณาข้อความเกี่ยวกับยางต่อไปนี้ ข้อใดถูก ก. ยาง
เกิดจากมอนอเมอร์ของธาตุซิลิคอน ข. ยางธรรมชาติ ทนต่อน้ำมันเบนซินและตัวละลายอินทรีย์
ค. การปรับปรุงคุณภาพยางธรรมชาติให้ดีขึ้น โดยนำมาคลุกกับกำมะถัน ง. ยาง SBR เกิดจากมอนอเมอร์ของสไตรีนและบิวทาไดอีน
1 : ก ข
2 : ข ค
3 : ค ง
4 : ก ง
ข้อที่ 8. ข้อใดกล่าวถูกต้อง ก. ปฏิกิริยาที่เกิดขึ้นแล้วให้พลังงานความร้อนออกมา
เรียกว่าปฏิกิริยาดูดความร้อน ข. ฝนกรดที่เกิดบริเวณที่มีการใช้ถ่านหิน
จะเกิดจากแก๊สคาร์บอนมอนออกไซด์ ค.โอโซน เป็นแก๊สพิษ
ทำให้เกิดการระคายเคืองกับดวงตาและทางเดินหายใจ ง.
โซเดียมไฮโดรเจนคาร์บอเนตหรือผงฟู ใช้ดับไฟป่าได้
1 : ก ข
2 : ข ค
3 : ค ง
4 : ก ง
ข้อที่ 9. พิจารณาข้อความต่อไปนี้
ข้อใดถูก ก. ซากพืชซากสัตว์ จะถูกย่อยสลายเกิดเป็นสารประกอบไฮโดรคาร์บอน ข.
ในการกลั่นลำดับส่วนน้ำมันดิบ จะได้สารที่เป็นแก๊สออกมาก่อน ค.
แก๊สหุงต้มในครัวเรือน ประกอบด้วยแก๊สมีเทนและโพรเพน ง. สารไฮโดรคาร์บอนอิ่มตัว
มีพันธะระหว่างคาร์บอนเป็นพันธะคู่
1 : ก ข
2 :
ข ค
4 :
ก ง
ข้อที่ 10. น้ำมันชนิดใดเหมาะกับเครื่องยนต์แก๊สโซลีนและไม่มีมลพิษ
ก. น้ำมันที่มีไอโซออกเทนมากกว่าเฮปเทนมากๆ ข.
น้ำมันที่มีการเติมสารเมทิลเทอร์เชียรีบิวทิลอีเทอร์ ค.
น้ำมันที่มีเลขออกเทนต่ำกว่า 75 และเติมสารเตตระเมทิลเลต ง.
น้ำมันที่มีเลขซีเทนสูงๆ
1 : ก ข
2 :
ข ค
3 :
ค ง
4 :
ก ง
ข้อที่ 11. สารชีวโมเลกุลชนิดใดมีมากที่สุดของน้ำหนักแห้งในร่างกายคน
1 : ไขมัน
2 : โปรตีน
3 : คาร์ไบไฮเดรต
4 : กรดนิวคลีอิก
ข้อที่ 12. ในการปรุงอาหารให้แก่ผู้สูงอายุควรหลีกเลี่ยงน้ำมันชนิดใด เพราะเหตุใด
2 : น้ำมันรำ เพราะเกิดกลิ่นเหม็นหืนง่าย
3 : น้ำมันมะพร้าว
เพราะมีกรดไขมันอิ่มตัวมาก
4 : น้ำมันเมล็ดดอกคำฝอย
เพราะมีกรดไขมันที่จำเป็นมาก
ข้อที่ 13. ข้อใดไม่ถูกต้อง
1 : กรดไลโนเลอิก
เป็นกรดไขมันชนิดไม่อิ่มตัว
2 : ถ้าเด็กทารกขาดกรดไลโนเลนิก
จะมีผิวหนังแห้ง อักเสบ หลุดลอก
3 : ไขมันเมื่อต้มกับเบสจะเกิดปฏิกิริยาสะปอนนิฟิเคชัน
4 : คอเลสเทอรอลไม่มีประโยชน์ต่อร่างกาย
ทำให้เส้นเลือดอุดตัน
ข้อที่ 14. กรดอะมิโนที่จำเป็นสำหรับทารกคือข้อใด
1: อาร์จินีน และฮีสติดีน
2 : ทริปโตเฟนและเมไทโอนีน
3 : ไลซีนและลิวซีน
4 : ไอโซลิวซีนและเวลีน
วันอาทิตย์ที่ 25 สิงหาคม พ.ศ. 2562
อุกกาบาตเท่า'ประตูชัย'มีโอกาส1ใน7,000ชนโลก ก.ย.นี้
ระทึก
นักวิทย์จับตา อุกกาบาตเท่า'ประตูชัย'มีโอกาส1ใน7,000ชนโลก
ก.ย.นี้
เมื่อ 24 มิ.ย.62 เว็บไซต์ มิร์เรอร์ รายงาน อุกกาบาต 2006 QV 89
ขนาดเท่า Arc de Triomphe ประตูชัยฝรั่งเศส ในกรุงปารีส
มีโอกาส 1 ใน 7,000
ที่จะพุ่งชนโลกของเรา ในเดือนกันยายน ที่จะถึงนี้ และหากอุกกาบาตนี้ชนจริง
จะก่อให้เกิดพลังทำลายล้างมากกว่า เหตุการณ์อุกกาบาตพุ่งชนโลก
โดยเกิดการระเบิดเหนือเมืองเชลยาบินสก์ ประเทศรัสเซีย ในปี 2556 ซึ่งองค์การบริหารการบินและอวกาศแห่งชาติสหรัฐฯ (นาซา)
ประมาณการว่าได้ปลดปล่อยพลังงานออกมาเท่ากับระเบิดทีเอ็นที 500 กิโลตัน
ตามรายงานของสำนักงานอวกาศยุโรป (ESA) คาดการณ์ว่าอุกกาบาต 2006 QV 89
ซึ่งมีขนาดเส้นผ่าศูนย์กลางประมาณ 40 เมตร
จะพุ่งผ่านโลกในวันที่ 9 ก.ย.62
และดูเหมือนระยะห่างจากโลก ใกล้ที่สุดอยู่ที่ราว 6.7
ล้านกิโลเมตร ทว่าถึงแม้จะห่างขนาดนี้ ก็ถือว่า อุกกาบาต 2006 QV 89 มีโอกาสชนโลกคิดเป็น 1 ใน7,299 เลยทีเดียว
ขณะที่ขนาดความกว้างของอุกกาบาต 2006 QV 89 อาจไม่ใหญ่มากพอที่จะทำลายล้างมนุษยชาติ แต่นักวิทยาศาสตร์ที่ ESA คาดการณ์ว่าหากอุกกาบาต 2006 QV 89 ชนโลกจริง
จะก่อให้เกิดพลังทำลายล้างมากกว่าตอนอุกกาบาต ขนาดความกว้าง 20 เมตร ระเบิดเหนือเมืองเชลยาบินสก์ เมื่อ ก.พ.56 ซึ่งก่อให้เกิดพลังทำลายล้างเท่ากับระเบิดปรมาณูที่ถล่มเมืองฮิโรชิมา
สมัยสงครามโลกครั้งที่ 2 ถึง 30 ลูก
ซึ่งแรงระเบิดของอุกกาบาตก่อให้เกิดช็อกเวฟ คลื่นกระแทก
ทำอาคารบ้านเรือนได้รับความเสียหายถึง 7,200 หลัง
และมีผู้คนได้รับบาดเจ็บกว่า 1,500 คน
วันศุกร์ที่ 23 สิงหาคม พ.ศ. 2562
3.2 พันธะไอออนิก
พันธะไอออนิก (
Ionic bond )
หมายถึง
พันธะระหว่างอะตอมที่อยู่ในสภาพอิออนที่มีประจุตรงกันข้ามกัน ซึ่งเกิดจากการเคลื่อนย้ายอิเล็กตรอน
11 ตัว หรือมากกว่า จากอิเล็กตรอนวงนอกสุดของอะตอมหนึ่งไปยังอีกอะตอมหนึ่ง
เพื่อให้จำนวนอิเล็กตรอนวงนอกสุด ครบออกเตต
ซึ่งเกิดขึ้นระหว่างอะตอมของโลหะกับอโลหะ
โดยที่โลหะเป็นฝ่ายจ่ายอิเล็กตรอนในระดับพลังงานชั้นนอกสุดให้กับอโลหะ
เนื่องจากโลหะมีค่าพลังงานไอออไนเซชันต่ำ
และอโลหะมีค่าพลังงานไอออไนเซชันสูง
ดังนั้นพันธะไอออนิกจึงเกิดขึ้นระหว่างโลหะกับอโลหะได้ดี กล่างคือ
อะตอมของโลหะให้เวเลนต์อิเล็กตรอนแก่อโลหะ แล้วเกิดเป็นไอออนบวกและไอออยลบของอโลหะ
เพื่อให้เวเลนต์อิเล็กตรอนเป็นแปด แบบก๊าซเฉื่อย
ส่วนอโลหะรับเวเลนต์อิเล็กตรอนมานั้นก็เพื่อปรับตัวเองให้เสถียรแบบก๊าซเฉื่อยเช่นกัน
ไอออนบวกกับไอออนลบจึงดึงดูดระหว่างประจุไฟฟ้าต่างกันเกิดเป็น สารประกอบ
ไอออนิก( Ionic
compuond) ดังนี้
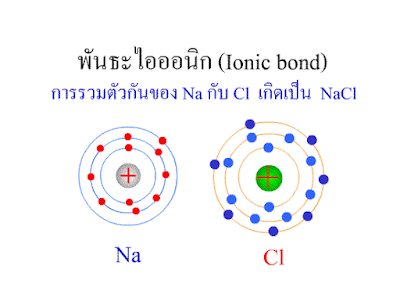
โซเดียมเสียอิเล็กตรอนให้แก่คลอรีน 1 ตัว
ทำให้อะตอมของโซเดียมมีเวเลนต์อิเล็กตรอน= 8
(อะตอมจะเสถียรเป็นไปตามกฎออกเตต)และทำให้มีจำนวนอิเล็กตรอนน้อยกว่าโปรตอน1ตัวทำให้อะตอมโซเดียมแสดงอำนาจไฟ
เป็นประจุบวก(+) ส่วนอะตอมคลอรีนรับอิเล็กจากโซเดียมมา 1 ตัวทำให้อะตอมของคลอรีนมีเวเลนต์อิเล็กตรอน=8(อะตอมเสถียรเป็นไปตามกฎออกเตต)
และทำให้มีจำนวนอิเล็กตรอนมากกว่าโปรตรอน 1 ตัว
ทำให้อะตอมคลอรีนแสดงอำนาจไฟฟ้าเป็นประลบ(-)
โซเดียมอิออนบวก(+) และคลอไรด์อิออน (-)
จะดึงดูดกัน เพราะมีประจุไฟฟ้าทีต่างกัน เกิดเป็น "พันธะไอออนิก"
อะตอมแมกนีเซียมมีการจัดเรียงอิเล็กตรอนเป็น
Mg = 2, 8, 2
แมกนีเซียมมีเวเลนต์อิเล็กตรอน = 2 ดังนั้น
แมกนีเซียมจะจ่ายอิเล็กตรอนให้แก่คลอรีนอะตอม 2 ตัว เพื่อให้เวเลนต์อิเล็กตรอนเป็น
8 จึงจะเสถียรเหมือนก๊าซเฉื่อย
ทำให้อะตอมของแมกนีเซียมมีจำนวนอิเล็กตรอนน้อยกว่าโปรตอน 2 ตัว
จึงแสดงอำนาจไฟฟ้าเป็นประจุ 2+
แมกนีเซียมไอออนบวก(Mq 2+)และคลอไรด์ไอออนลบ(Cl -) จะเกิดแรงดึงดูดกัน
เพราะมีประจุไฟฟ้าต่างกันเป็นโมเลกุลของแมกนีเซียมคลอไรด์
การเกิดพันธะไอออนิกในสารประกอบ
แบเรียมออกไซด์ ( BaO )
การจัดเรียงอิเล็กตรอนของแบเรียม Ba = 2, 8, 18, 18, 8, 2
( Ba มีเวเลนต์อิเล็กตรอน = 2) และการจัดเรียงอิเล็กตรอนของออกซิเจน O =
2, 6
( O มีเวเลนต์อิเล็กตรอน = 6 ) Ba เสียอิอล็กตรอนให้ O
จำนวน 2 ตัว Ba จึงมีประจุเป็น 2+ ส่วน O
ได้รับอิเล็กตรอนมา2 ตัว จึงมีประจุไฟฟ้าเป็น 2-
เกิดแรงยึดเหนี่ยวด้วยประจุไฟฟ้าต่างกัน เป็นโมเลกุลของแบเรียมออกไซด์
1. พันธะไอออนิกเป็นพันธะที่เกิดจาก
ไอออนของโลหะ + ไอออนของอโลหะ เช่น NaCl, MgO, KI
2. พันธะไอออนิก
อาจเป็นพันธะเคมีที่เกิดจากธาตุที่มีค่าพลังงานไอออไนเซชันต่ำกับธาตุที่มีค่าพลังงานไอออไนเซชันสูง
3. พันธะไอออนิก
อาจเป็นพันธะที่เกิดจากไอออบวกที่เป็นกลุ่มอะตอมของอโลหะ เช่น
4. สารประกอบไอออนิกไม่มีสูตรโมเลกุล
มีแต่สตรเอมพิริคัล ( สูตรอย่างง่าย )
5.สารประกอบไอออนิกมีจุดดือดและจุดหลอมเหลวสูง
6. สารประกอบไอออนิกในภาวะปกติเป็นของแข็ง
ประกอบไอออนบวกและไอออนลบ ไอออนเหล่านี้ไม่เคลื่อนที่ ดังนั้นจึงไม่นำไฟฟ้า
แต่เมื่อหลอมเหลวหรือละลายน้ำ จะแตกตัวเป็นอิออนและเคลื่อที่ได้
เกิดเป็นสารอิเล็กโทรไลดต์จึงนำไฟฟ้าได้
โครงสร้างของสารประกอบไอออนิก
โครงสร้างของสารประกอบไอออนิกมีลักษณะเป็นโครงผลึกร่างตาข่าย
ประกอบด้วยไอออนบวกและไอออนลบสลับกัน ไม่สามารถแบ่งแยกเป็นโมเลกุลเดี่ยวๆได้
ดังนั้นจึงไม่สามารถทราบขอบเขตของไอออนของธาตุต่างๆใน 1 โมเลกุลได้
แต่สามารถหาอัตราส่วนอย่างต่ำของไอออนที่เป็นองค์ประกอบเท่านั้น
จึงไม่สามารถเขียนสูตรโมเลกุลของสารประกอบไอออนิกได้ ใช้สูตรเอมพิริคัลแทนสูตรเคมีของสารประกอบไอออนิก
สารประกอบไอออนิก
เมื่อโลหะทำปฏิกิริยากับอโลหะ
ธาตุทั้งสองจะรวมกันด้วยพันธะไอออนิกเกิดเป็นสารประกอบไอออนิก
โดยอะตอมของโลหะจะให้(จ่าย,เสีย)เวเลนต์อิเล็กตรอนแก่อะตอมของอโลหะ
ดังนั้นธาตุหมู่ 1A ซึ่งมีเวเลนต์อิเล็กตรอนเท่ากับ 1
จึงเกิดเป็นไอออนที่มีประจุ +1 ธาตุหมู่ 2 ซึ่งมีเวเลนต์อิเล็กตรอนเท่ากับ 2
เมื่อเกิดเป็นไอออนจะมีประจุ +2 เป็นต้น
ส่วนอโลหะซึ่งมีจำนวนเวเลนต์อิเล็กตรอนใกล้เคียงกับก๊าซเฉื่อยจะรับอิเล็กตรอนมาให้ครบแปด
เช่น ธาตุหมู่ 7A จะรับอิเล็กตรอน 1 ตัว
เมื่อกลายเป็นไอออนจะมีประจุ -1 สำหรับธาตุหมู่ 5 และหมู่ 6 เมื่อเกิดเป็นไอออนจะมีประจุ
-3 และ -2ตามลำดับ เนื่องจากสามารถรับอิเล็กตรอนได้ 3 และ 2
อิเล็กตรอนแล้วมีการจัดเรียงอิเล็กตรอนตามกฎออกเตต
การเขียนสูตรและการเรียกชื่อสารประกอบไอออนิก
ธาตุหมู่
I
II
II
IV
V
VI
VII
ประจุบนไอออน
+1
+2
+3
-4
-3
-2
-1
ก. การเขียนสูตรสารประกอบไอออนิก
ใช้หลักดังนี้
1.
เขียนไอออนบวกของโลหะหรือกลุ่มไอออนบวกไว้ข้างหน้า
ตามด้วยไอออนลบของอโลหะหรือกลุ่มไอออนลบ
2. ไอออนบวกและไอออนลบ
จะรวมกันในอัตราส่วนที่ทำให้ผลรวมของประจุเป็นศูนย์
ดังนั้นจึงต้องหาตัวเลขมาคูณกับจำนวนประจุบนไอออนบวกและไอออนลบให้มีจำนวนเท่ากัน
แล้วใส่ตัวเลขเหล่านั้นไว้ที่มุมขวาล่างของแต่ละไอออน
ซึ่งทำได้โดยใช้จำนวนประจุบนไอออนบวกและไอออนลบคูณไขว้กัน
3. ถ้ากลุ่มไอออนบวกหรือไอออนลบมีมากกว่า 1
กลุ่ม ให้ใส่วงเล็บ ( ) และใส่จำนวนกลุ่มไว้ที่มุมล่างขวาล่าง ดังตัวอย่าง
จงเขียนสูตรของสารประกอบไอออนิกต่อไปนี้
ก. Na+ กับ O2- ข. Ca2+ กับ Cl-
ค. NH4+ กับ SO42-
ข. การอ่านชื่อสารประกอบไอออนิก
1. สารประกอบธาตุคู่ ถ้าสารประกอบเกิดจาก
ธาตุโลหะที่มีไอออนได้ชนิดเดียวรวมกับอโลหะ ให้อ่านชื่อโลหะที่เป็นไอออนบวก
แล้วตามด้วยชื่อธาตุอโลหะที่เป็นไอออนลบ โดยเปลี่ยนเสียงพยางค์ท้ายเป็น ไอด์ (ide) เช่น
-ออกซิเจน เปลี่ยนเป็น ออกไซด์ (oxide)
-ไฮโดรเจน เปลี่ยนเป็น ไฮไดรด์ (hydride)
-คลอรีน เปลี่ยนเป็น คลอไรด์ (chloride)
-ไอโอดีน เปลี่ยนเป็น ไอโอไดด์ (iodide)
NaCl อ่านว่า โซเดียมคลอไรด์ (Sodium chloridr)
CaI2 อ่านว่า แคลเซียมไอโอไดด์ (Calcium iodide)
KBr อ่านว่า โพแทสเซียมโบรไมด์ (Potascium bromide)
CaCl2 อ่านว่า แคลเซียมคลอไรด์ (Calcium chloride)
ตัวอย่างการอ่านชื่อสารประกอบไอออนิกธาตุคู่
ถ้าสารประกอบที่เกิดจากธาตุโลหะเดีนวกันที่มีไอออนได้หลายชนิด
รวมตัวกับอโลหะ
ให้อ่านชื่อโลหะที่เป็นไอออนบวกแล้วตามด้วยค่าประจุของไอออนของโลหะโดยวงเล็บเป็นเลขโรมัน
แล้วตามด้วยอโลหะที่เป็นไอออนลบ โดยเปลี่ยนเสียงพยางค์ท้ายเป็น ไอด์ (ide) เช่น Fe เกิดไอออนได้ 2 ชนิดคือ Fe 2+ และ Fe 3+ และCu เกิดอิออนได้
2 ชนิดคือ Cu + และ Cu 2+
สารประกอบที่เกิดขึ้นและการอ่านชื่อ ดังนี้
FeCl2 อ่านว่า ไอร์ออน (II) คลอไรด์ ( Iron (II)
chloride )
CuS อ่านว่า คอปเปอร์ (I) ซัลไฟด์ ( Cupper (I)
sunfide )
FeCl3 อ่านว่า ไอร์ออน (III) คลอไรด์ ( Iron
(III) chloride )
Cu2S อ่านว่า คอปเปอร์ (II) ซัลไฟด์
( Copper (II) sunfide )
2. สารประกอบธาตุสามหรือมากกว่า
ถ้าสารประกอบเกิดจากไอออนบวกของโลหะ หรือกลุ่มไอออนบวกรวม
ตัวกับกลุ่มไอออนลบ
ให้อ่านชื่อไอออนบวกของโลหะหรือชื่อกลุ่มไอออนบวก แล้วตามด้วยกลุ่มไอออนลบ เช่น
CaCO3 อ่านว่า แคลเซียมคาร์บอนเนต (Calcium carbonatX
KNO3 อ่านว่า โพแทสเซียมไนเตรต (Potascium nitrae)
Ba(OH)2 อ่านว่า แบเรียมไฮดรอกไซด์ (Barium hydroxide)
(NH4)3PO4 อ่านว่า แอมโมเนียมฟอสเฟต (Ammomium
pospate)
การละลายของสารประกอบไอออนิก
สารประกอบไอออนิกบางชนิดละลายน้ำได้ดีและบางชนิดไม่ละลายน้ำ
การที่สารประกอบไอออนิกละลายน้ำได้เนื่องจากแรงดึงดูดระหว่างโมเลกุลของน้ำกับไอออนมีค่ามากกว่าแรงยึดเหนี่ยวระหว่างไอออนบวกกับไอออนลบ
เช่น เมื่อนำโซเดียมคลอไรด์มาละลายในน้ำ แรงดึงดูดระหว่างโมเลกุลของน้ำกับโซเดียมไอออน
และน้ำกับคลอไรด์ไอออนมีค่าสูงกว่าแรงยึดเหนี่ยวระหว่างไอออนทั้งสอง
โซเดียมคลอไรด์จึงละลายน้ำได้ เมื่อไอออนเหล่านี้หลุดออกจากโครงสร้างเดิม
แต่ละไอออนจะถูกล้อมรอบด้วยโมเลกุลของน้ำหลายๆโมเลกุล
โดยน้ำจะหันขั้วที่มีประจุตรงกันข้ามเข้าไอออนที่ล้อมรอบ
ในการละลายน้ำของสารประกอบไอออนิก
จะมีขั้นย่อยๆของการเปลี่ยนแปลง 2 ขั้นตอน ดังนี้
ขั้นที่ 1
ผลึกของสารประกอบไอออนิกสลายตัวออกเป็นไอออนบวกและลบในภาวะก๊าซ
ขั้นนี้ต้องใช้พลังงานเพื่อสลายผลีก พลังงานนี้เรียกว่า พลังงานโครงร่างผลึก ( latece energy
) , E1
ขั้นที่ 2
ไอออนบวกและไอออนลบในภาวะก๊าซรวมตัวกับน้ำ ขั้นนี้มีการคายพลังงาน
พลังงานที่คายออกมาเรียกว่า พลังงานไฮเดรชัน (Hydration energy ) , E2
พลังงานของการละลาย ( D E) มีค่า = E1 + E2
พลังงานของการละลายพิจารณาจากพลังงานโครงร่างผลึก ( E1 )
และพลังงานไฮเดรชัน( E2 ) ดังนี้
1.ถ้าค่า D E< 0 ( E1 < E2 ) การละลายจะเป็นแบบคายพลังงาน
2.ถ้าค่าD E > 0 ( E1 > E2 ) การละลายจะเป็นแบบดูดพลังงาน
3.ถ้าD E = 0 ( E1
= E2 ) การละลายจะไม่คายพลังงาน
4.ถ้า พลังงานโครงร่างผลึกมีค่ามากกว่าพลังงานไฮเดรชันมากๆ
( E1 >>>> E2 ) จะไม่ละลายน้ำ
สมัครสมาชิก:
ความคิดเห็น (Atom)
-
จากการศึกษาแบบจำลองอะตอมโดยใช้สมการทางคณิตศาสตร์ขั้นสูงที่เรียกว่าสมการคลื่น คำนวณหาค่าพลังงานของอิเล็กตรอน ทำให้ทราบว่าอะตอมประกอบด้วยโปร...
-
พันธะไอออนิก ( Ionic bond ) หมายถึง พันธะระหว่างอะตอมที่อยู่ในสภาพอิออนที่มีประจุตรงกันข้ามกัน ซึ่งเกิดจากการเคลื่อนย้ายอิเล็กตรอน ...
-
แบบจำลองอะตอมของ จอร์น ดอลตัน ในปี พ.ศ. 2346 ( ค.ศ. 1803) จอห์น ดอลตัน ( John Dalton) นักวิทยาศาสตร์ชาวอังกฤษได้เสนอทฤษฎีอะตอม เ...